丂偙偺復偱偼丆惗惉擬傗寢崌僄僱儖僊乕偵偮偄偰妛傃傑偟傚偆丅偙偺復偺撪梕傕丆僿僗偺朄懃偲娭學偑偁傝傑偡丅
丂偙偺復偱偼丆惗惉擬傗寢崌僄僱儖僊乕偵偮偄偰妛傃傑偟傚偆丅偙偺復偺撪梕傕丆僿僗偺朄懃偲娭學偑偁傝傑偡丅 侾丏扨懱偲偼壗偱偡偐? 偦傟埲忋嵶偐偄惉暘偵暘偗傞偙偲偺偱偒側偄弮暔幙偺偙偲傪偄偆丅 扨懱偼丆侾庬椶偺尦慺偱偱偒偨弮暔幙偱偁傞丅 俀丏嫟桳寢崌偲偼丆偳偺傛偆側寢崌偱偡偐? 尨巕娫偱弌偟崌偭偨壙揹巕傪嫟桳偟偰偱偒傞寢傃偮偒偺偙偲傪偄偆丅丂 |
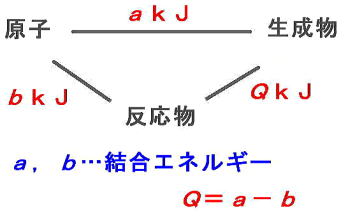
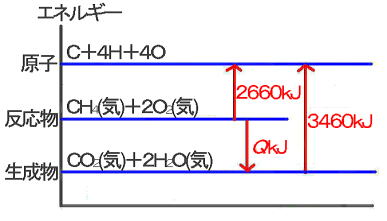
丂寢崌僄僱儖僊乕偼丆壔妛 俬俬 偱埖偆撪梕偱偡偑丆偙偙偱徯夘偟偰偍偒傑偡丅寢崌僄僱儖僊乕偼丆嫟桳寢崌傪愗傞偨傔偵昁梫側僄僱儖僊乕偱偡丅偙偺寢崌僄僱儖僊乕傪巊偭偰傕丆斀墳擬傪媮傔傞偙偲偑偱偒傑偡丅
丂丂
 丂丂
丂丂丂偙偺復偺妛廗撪梕偼丆師偺捠傝偱偡丅
乮侾乯惗惉擬
乮俀乯寢崌僄僱儖僊乕
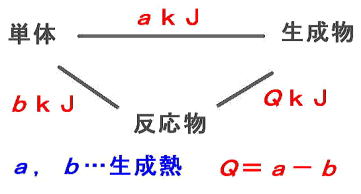
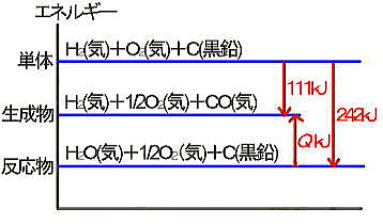
丂偱偼丆惗惉擬偐傜偼偠傔傑偟傚偆丅扨懱偺惗惉擬偑侽偵側傞偙偲偵拲堄偟偰偔偩偝偄丅丂




 丂
丂




 丂
丂