丂偙偺復偱偼丆巁壔娨尦斀墳偵偮偄偰挷傋傞幚尡傪徯夘偟傑偡丅偦偺慜偵丆巁壔嵻偲娨尦嵻偵偮偄偰暅廗偟偰偍偒傑偟傚偆丅
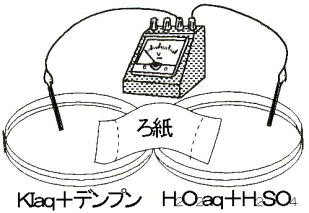
丂偙偺復偱偼丆巁壔娨尦斀墳偵偮偄偰挷傋傞幚尡傪徯夘偟傑偡丅偦偺慜偵丆巁壔嵻偲娨尦嵻偵偮偄偰暅廗偟偰偍偒傑偟傚偆丅 侾丏巁壔嵻偲偼壗偱偡偐? 巁壔娨尦斀墳偵偍偄偰丆揹巕傪扗偄丆憡庤偺暔幙傪巁壔偡傞暔幙偺偙偲傪偄偆丅 俀丏娨尦嵻偲偼壗偱偡偐? 巁壔娨尦斀墳偵偍偄偰丆揹巕傪梌偊丆憡庤偺暔幙傪娨尦偡傞暔幙偺偙偲傪偄偆丅 |
丂師偵丆儓僂壔暔僀僆儞俬亅偑巁壔偝傟偰儓僂慺暘巕俬俀偵側傞偲丆傕偪傠傫怓偺曄壔偑偁傝傑偡丅偟偐偟丆偦傟偩偗偱偼側偔丆儓僂慺僨儞僾儞斀墳偵傛偭偰儓僂慺暘巕傪妋擣偡傞偙偲偑偱偒傑偡偹丅
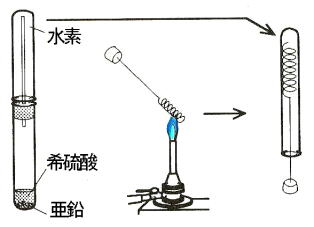
丂傑偨丆怓偺曄壔偑側偔偰傕丆巁壔偝傟傞偲婥懱偑敪惗偡傞傕偺傕偁傝傑偡丅僔儏僂巁乮俠俷俷俫乯俀偑巁壔偝傟傞偲擇巁壔扽慺俠俷俀偑敪惗偟傑偡丅夁巁壔悈慺俫俀俷俀偑巁壔偝傟傞偲巁慺俷俀傪敪惗偟傑偡丅偟偐偟丆婥懱偺敪惗偼彮検偱偁傝丆媫寖側偨傔拲堄偟側偗傟偽偄偗傑偣傫丅
 丂
丂