 過酸化水素を触媒を使って分解すると,水と酸素になります。この反応で発生した酸素の体積から,反応速度を求めることができます。
過酸化水素を触媒を使って分解すると,水と酸素になります。この反応で発生した酸素の体積から,反応速度を求めることができます。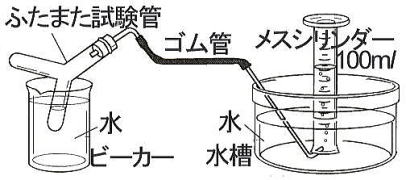
この章の学習内容は,次の通りです。
(1)水蒸気圧の影響
(2)分解された過酸化水素の物質量
(3)過酸化水素水の濃度の変化量
(4)反応速度
それでは,最初に水蒸気圧の影響のついて検討しましょう。
 1.蒸気圧とは何ですか? 密閉容器内に適当量の水を入れて放置すると,その上部の空間に蒸発した水蒸気が,一定温度では一定の圧力を示すようになる。このとき,上部の空間には水蒸気が飽和した状態になっている。このときの圧力を水の蒸気圧と言う。 2.分圧の法則とはどのようなものでしたか? 混合気体の全圧は,各成分気体の分圧の和に等しい。1801年にイギリスのドルトンが発見した。 3.過酸化水素を分解すると,何が生成しますか? 水と酸素ができる。 |




